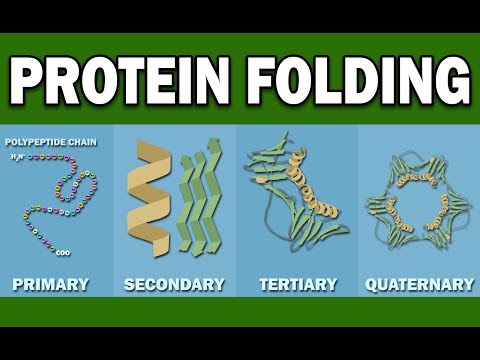
アルファヘリックスとベータプリーツシート
コンテンツ
モチーフはタンパク質の二次構造に位置し、らせんの区別を与えるコイル状またはらせんの右側の確認として標準になります。したがって、一般的にはアルファらせんとして知られています。一方、βシートとも呼ばれるベータプリーツシートは、タンパク質に存在する特徴的な二次構造の標準モチーフとして定義されます。

内容:Alpha HelixとBetaプリーツシートの違い
- 比較表
- Alpha Helixとは何ですか?
- ベータプリーツシートとは何ですか?
- 主な違い
- ビデオ説明
比較表
| 区別の基礎 | アルファヘリックス | ベータプリーツシート |
| 定義 | モチーフはタンパク質の二次構造に位置し、らせんの区別を与えるコイル状またはらせん状の右側の確認として標準になります。 | bシートとも呼ばれるベータプリーツシートは、タンパク質に存在する特徴的な二次構造の標準モチーフとして定義されます。 |
| アミノ酸 | アミノ酸の-Rグループは外側の表面に存在します。 | -Rグループは、シートの外側と内側の表面に存在します。 |
| ボンディング | らせん構造を作成するために、水素結合がポリペプチド鎖内に作成されます。 | 水素結合からの2つ以上のベータストランドのリンクによって存在します。 |
Alpha Helixとは何ですか?
モチーフはタンパク質の二次構造に位置し、らせんの区別を与えるコイル状またはらせんの右側の確認として標準になります。したがって、一般的にはアルファらせんとして知られています。ここで、構造内で、N-H基は、タンパク質の配列の4残基前に存在するアミノ酸の骨格と呼ばれるC = O基への水素結合を示します。現在のαヘリックスの実証における2つの重要な進歩は、次のとおりです。アミノ酸とペプチドの宝石構造の判断のための正しい結合ジオメトリと、平面ペプチド結合のポーリングの期待。そして、彼はヘリックスのターンごとに必要な数の預金の疑いをあきらめました。 1948年の早春、ポーリングがバグを抱えて寝てしまったときに、重要な瞬間が訪れました。使い果たされた彼は、一枚の紙にほぼ正しい測定値のポリペプチド鎖を描き、それをらせんに折り畳み、平面ペプチド結合を維持することに留意した。アルファヘリックスは、自然界で最もよく知られているヘリックスです。それは、アミノ酸の側鎖が中心から外側に広がる創傷ポリペプチド鎖から成り、これによりその形状を維持することが可能になる。それらは、例えばミオグロビンなどの球状タンパク質から、糸状タンパク質であるケラチンまで、広範囲の種類のタンパク質に見られます。特権を付与するか、左巻きのヘリックスにすることができますが、サイドチェーンが競合しないため、アルファヘリックスループがサポートされていることが実証されています。この情報は、アルファヘリックスの安定性を示します。アルファヘリックスカールの各ターンには3.6のアミノ腐食性堆積物があります。
ベータプリーツシートとは何ですか?
bシートとも呼ばれるベータプリーツシートは、タンパク質に存在する特徴的な二次構造の標準モチーフとして定義されます。他のタンパク質との違いは、プリーツシートを形成する構造内に存在する水素原子の少なくとも2つまたは3つとのつながりを持つ鎖で構成される要因になります。 βストランドは、3から10アミノ酸の長さのポリペプチドアンカーの範囲であり、脊椎の適応が広くなっています。 βシートの超分子の関係は、多くの人間の病気、特にアルツハイマー病などのアミロイドーシスに見られるタンパク質の総量と原線維の配列に巻き込まれています。この構造は、ポリペプチド鎖の2つの部分がお互いを覆い、互いに水素結合の線を形作るときに起こります。このアクションは、パラレルアクションコースまたはパラレルプランと敵対的に発生する可能性があります。同じゲーム計画と並行して、それはポリペプチド鎖の方向性の即時の結果です。ベータしわシートに対応する構造は、αしわシートです。この構造は、β-折り目が付けられたシートよりも熱狂的に理想的ではなく、タンパク質では本当に前例のないものです。 α折り目が付けられたシートは、そのカルボニルとアミノの集まりの配置によって記述されます。カルボニル基はすべて1つの見出しで調整され、すべてのN-H集合は他の方法で調整されます。
主な違い
- モチーフはタンパク質の二次構造に位置し、らせんの区別を与えるコイル状またはらせんの右側の確認として標準になります。したがって、一般的にはアルファらせんとして知られています。一方、βシートとも呼ばれるベータプリーツシートは、タンパク質に存在する特徴的な二次構造の標準モチーフとして定義されます。
- アミノ酸の-R基はらせんの外側の表面に存在しますが、-R基はシートの外側と内側の表面に存在します。
- アルファヘリックスは、水素結合によって保持された、スプリングのような構造にポールモールドされて巻かれたポリペプチドチェーンです。一方、ベータプリーツシートは、脊椎を形成する少なくとも2つの水素結合によって側面に沿って関連付けられたベータストランドで作られます。
- らせんは、左巻き(ベータ)または右巻きで、αらせんは常に右巻きです。それどころか、チェーンは、ベータプリーツシートで互いに逆に配置された他の文字列に隣接して調整されます。
- アルファらせんの形成は、らせん構造を作成するために水素結合がポリペプチド鎖内で作成されるように存在します。一方、ベータプリーツシートは、水素結合からの2つまたは2つ以上のベータストランドのリンクによって存在します。