共有結合とイオン結合

コンテンツ
イオン結合と共有結合の主な違いは、電子対と原子の共有です。共有結合では、イオン結合中に原子は互いに静電的に引き付けられます。電子対は原子間で共有されます。
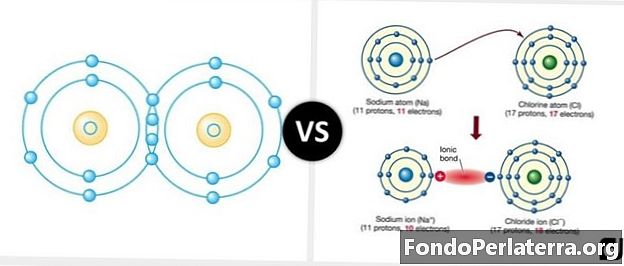
内容:共有結合とイオン結合の違い
- 比較表
- 共有結合とは何ですか?
- イオン結合とは何ですか?
- 主な違い
- ビデオ説明
比較表
| 区別の基礎 | 共有結合 | イオン結合 |
| 定義 | 共有結合は、原子間で共有ペアまたは結合ペア(電子ペア)を共有することを含む化学結合の一種です。 | イオン結合は、1つの原子から別の原子への1つまたは複数の電子の共有または完全な放棄を伴う化学結合のタイプです。 |
| 発生 | 共有結合は中性原子の相互作用の結果です | イオン結合は、陰イオンと陽イオンの相互作用の結果です。 |
| 化学ポテンシャル | これらは非常に弱い化学結合です | これらは最強の化学結合です。 |
| 形成 | 非金属元素は共有結合を形成します | 金属元素はイオン結合を形成します |
| 電子状態 | 共有電子 | 電子の総移動 |
| 物質の状態 | 室温での液体と気体 | 室温での固体 |
| 化合物 | オーガニック | 無機 |
| 溶解度 | 水に不溶 | 水に可溶 |
| 形状 | 明確な形状 | 明確な形状なし |
| ネーミング | ギリシャ語の接頭辞 | ローマ数字 |
| 例 | 塩酸とメタン | 硫酸と塩化ナトリウム |
共有結合とは何ですか?
共有結合は分子結合とも呼ばれ、原子間で共有ペアまたは結合ペア(電子ペア)を共有する化学結合の種類です。ほとんどの分子では、電子の共有により、各原子は安定した電子配置に対応する完全な外殻に相当するものを取得できます。原子が電子に対して同様の親和性を持っている場合、電子に対する親和性が同じであり、原子によってそれらを提供する傾向がないため、共有結合が発生する可能性があります。原子は電子を共有してオクテット配置を獲得し、より安定して強くなります。シグマ軌道とパイ軌道の相互作用により、共有結合は4種類の結合、すなわち、単一、二重、三重、および四重結合を形成できます。酸素原子は、閉じた殻を形成するために2つの追加の電子を必要とする最良の例ですが、水素原子は閉じた殻を形成するために1つ必要です。酸素原子は水素原子と2つの電子を共有するため、両方の原子は閉じた殻を持っています。これにより、最終的に水分子が作成されます。
イオン結合とは何ですか?
イオン結合は、1つの原子から別の原子への1つまたは複数の電子の共有または完全な放棄を伴う化学結合のタイプです。イオン結合は、電子を失いやすい要素と電子を獲得する要素の結果です。これらのタイプの結合は、クーロンの法則で説明されているように、電荷間の相互作用のために分子にはまったく関係しません。イオン結合は室温で固体のままです。何十億ものイオンが形成される周期的な格子の間に、各イオンは反対電荷の多くのイオンに囲まれているためです。負イオンと正イオン間の静電引力により、化合物が結合します。イオン結合プロセス中の全体のエネルギーは通常正であり、反応が吸熱性であり、好ましくないことを示します。一方、この反応は、静電引力のために同時に好ましい。イオン結合の一般的な例は、ナトリウムまたは塩です。ナトリウム原子はすぐに電子を与え、その結果正電荷が生じます。塩素はこれらの電子を受け取り、負に帯電します。これらの2つの反対に帯電した原子は、互いに引き付けられて塩化ナトリウム分子を形成します。
主な違い
- 共有結合では、電子軌道は重なり合っていますが、イオン結合の場合は別々です。
- 共有結合は、硬くて脆いイオン結合と比較して比較的柔らかいです。
- 金属原子と非金属原子の両方が、共有結合の形成中にイオン結合の形成に関与しています。非金属原子のみが関与します。
- 電子の共有のために共有結合が形成され、電子の移動のためにイオン結合の形成が発生します。
- 分子は化合物の形成中に共有結合した粒子であり、イオン結合ではこれらは正に帯電したイオンと負に帯電したイオンです。
- 共有結合は非伝導体であり、イオン結合は伝導体です。
- 電気陰性度がほとんど異なる原子間で共有結合が発生します。電気陰性度が大きく異なる原子間では、イオン結合が起こります。
- イオン結合の場合、イオン結合には高融点と沸点が必要です。共有結合の場合、共有結合には低融点と低沸点が必要です。
- メタンと塩酸は、共有結合の塩化ナトリウムの一般的な例であり、硫酸はイオン結合の例です。
- 共有結合の形状は明確ですが、イオン結合の形状は明確ではありません
- 共有結合は極性が低く、イオン結合は極性が高いです。
- 100%の共有分子は油に溶けますが、水には溶けませんが、多くのイオン結合は水には溶けますが、油には溶けません。
- 炭素分子は主に共有結合を介して相互作用するため、共有結合は重要です。一方、イオン結合は特定の有機化合物の合成を可能にするため重要です。
- 共有結合は元素と化合物の両方であり、イオン結合は化合物のみです。





